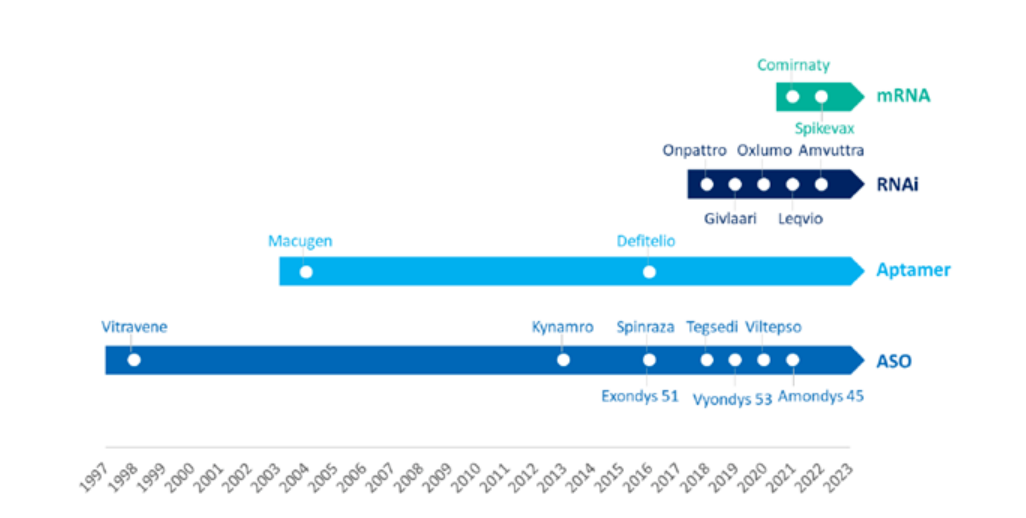
Дереккөз: WuXi AppTec
Соңғы жылдары РНҚ терапиясының саласы жарылыс тенденциясын көрсетті.Тек соңғы 5 жылда 11 РНҚ терапиясы FDA мақұлдаған және бұл сан тіпті бұрын бекітілген РНҚ терапиясының қосындысынан асып түседі!Дәстүрлі терапиямен салыстырғанда, РНҚ терапиясы мақсаттың гендік тізбегі белгілі болған кезде жоғары табыстылықпен мақсатты терапияны тез дамыта алады.Екінші жағынан, РНҚ терапиясының көпшілігі әлі де сирек кездесетін ауруларды емдеу үшін ғана қол жетімді және мұндай терапияны дамыту әлі де терапияның ұзақтылығы, қауіпсіздігі және жеткізілуі тұрғысынан көптеген қиындықтарға тап болады.Бүгінгі мақаладаWuXi AppTec контент командасы өткен жылы РНҚ терапиясы саласындағы прогресті қарастырады және оқырмандармен бірге осы дамып келе жатқан саланың болашағын күтеді.
▲ Соңғы 5 жылда 11 РНҚ терапиясы немесе вакцина FDA мақұлдаған
Сирек кездесетін аурулардан жалпы ауруларға дейін көбірек гүлдер гүлдейді
Жаңа тәждік індетте мРНҚ вакцинасы күтпеген жерден пайда болды және өнеркәсіптен кеңінен назар аударды.Кейінжұқпалы ауруларға қарсы вакциналарды жасаудағы серпіліс, мРНҚ технологиясының алдында тұрған тағы бір маңызды мәселе - көбірек ауруларды емдеу және алдын алу үшін қолдану аясын кеңейту.
Олардың арасында,Қатерлі ісікке қарсы жеке вакциналар mRNA технологиясының маңызды қолдану саласы болып табылады, және біз сондай-ақ осы жылы бірнеше қатерлі ісікке қарсы вакциналардың оң клиникалық нәтижелерін көрдік.Дәл осы айда Модерна мен Мерк бірлесіп әзірлеген, Кейтруда PD-1 ингибиторымен біріктірілген қатерлі ісікке қарсы жеке вакцина,тәуекелді азайттыІсікті толық резекциялаудан кейін III және IV сатыдағы меланомасы бар науқастарда қайталану немесе өлім 44%-ға (Кейтруда монотерапиясымен салыстырғанда).Баспасөз релизінде бұл мРНҚ қатерлі ісігіне қарсы вакцина рандомизацияланған клиникалық сынақта меланоманы емдеудегі тиімділігін алғаш рет көрсеткені, бұл мРНҚ қатерлі ісігіне қарсы вакциналарды жасаудағы маңызды оқиға екенін атап өтті.
Сонымен қатар, мРНҚ вакциналары жасушалық терапияның емдік әсерін күшейте алады.Мысалы, BioNTech зерттеуі пациенттерге CLDN6-мақсатты CAR-T терапиясының төмен дозасын бірінші рет енгізетінін көрсетті.BNT211, содан кейін CLDN6 кодтайтын мРНҚ вакцинасымен енгізіледі, олар антигенді ұсынатын жасушалардың бетінде CLDN6 экспрессиясы арқылы CAR-T жасушаларын in vivo ынталандыра алады.Күшейту, осылайша ісікке қарсы әсерді күшейтеді.Алдын ала нәтижелер біріктірілген ем қабылдаған 5 пациенттің 4-і жартылай немесе 80% жауапқа қол жеткізгенін көрсетті.
Аурулардың ауқымын кеңейтуде мРНҚ терапиясынан басқа, олигонуклеотидтік терапия және РНҚ терапиясы да жақсы нәтижелерге қол жеткізді.Созылмалы В гепатитін емдеуде пациенттердің 30%-ға жуығы антисенс олигонуклеотидті терапияны қолданғаннан кейін В гепатитінің беткі антигенін және В гепатиті вирусының ДНҚ-сын in vivo анықтай алмайды.GSK және Ionis бірлесіп әзірлеген bepirovirsen24 апта бойы.Кейбір емделушілерде емдеуді тоқтатқаннан кейін де 24 аптадан кейін де В гепатитінің бұл маркерлері денеде әлі анықталмады.
Кездейсоқ, RNAi терапиясыVir Biotechnology және Alnylam бірлесіп жасаған VIR-2218 біріктірілдіα интерферонымен және 2-фазалық клиникалық зерттеулерде созылмалы В гепатиті бар науқастардың шамамен 30%-ы да В гепатитінің беткі антигенін (HBsAg) анықтай алмады.Сонымен қатар, бұл пациенттерде иммундық жүйенің оң реакциясын көрсететін В гепатиті ақуызына қарсы антиденелер дамыды.Осы нәтижелерді біріктіре отырып, сала РНҚ терапиясы В гепатитін функционалды емдеудің кілті болуы мүмкін екенін көрсетеді.
Бұл жалпы ауруларға арналған РНҚ терапиясының бастамасы ғана болуы мүмкін.Alnylam's R&D құбырына сәйкес, ол сонымен қатар гипертонияны, Альцгеймер ауруын және алкогольсіз стеатогепатитті емдеуге арналған RNAi терапиясын әзірлеуде және болашақты асыға күтуге тұрарлық.
РНҚ терапиясын жеткізудің тар мойнынан өту
РНҚ терапиясын жеткізу оны қолдануды шектейтін кедергілердің бірі болып табылады.Сондай-ақ ғалымдар РНҚ терапиясын бауырдан басқа мүшелер мен тіндерге арнайы жеткізу үшін әртүрлі технологияларды әзірлеуде.
Потенциалды әдістердің бірі терапевтік РНҚ-ны тінге тән молекулалармен «байланыстыру» болып табылады.Мысалы, жақында Avidity Biosciences өзінің технологиялық платформасы моноклоналды антиденелерді олигонуклеотидтерге біріктіре алатынын хабарлады.siRNA-ны тиімді байланыстырады.қаңқа бұлшықетіне жіберіледі.Баспасөз релизінде бұл siRNA-ны адамның бұлшықет тініне сәтті бағыттауға және жеткізуге болатын бірінші рет екенін, бұл РНҚ терапиясы саласындағы үлкен серпіліс екенін атап өтті.
Сурет көзі: 123RF
Антиденелерді конъюгациялау технологиясымен қатар, липидті нанобөлшектерді (LNP) әзірлейтін бірқатар компаниялар да осындай тасымалдаушыларды «жаңартуда».Мысалы, ReCode Therapeuticөкпеге, көкбауырға, бауырға және басқа мүшелерге РНҚ терапиясының әртүрлі түрлерін жеткізу үшін өзінің бірегей Селективті органды мақсатты LNP технологиясын (SORT) пайдаланады.Биыл компания инвестицияға Pfizer, Bayer, Amgen, Sanofi және басқа да ірі фармацевтикалық компаниялардың венчурлық капитал департаменттері қатысатын 200 миллион АҚШ доллары көлеміндегі B сериялы қаржыландыру кезеңін аяқтағанын хабарлады.Биылғы жылы A сериясы бойынша 25 миллион доллар қаржы алған Kernal Biologics сонымен қатар бауырда жиналмайтын, бірақ ми немесе нақты ісік сияқты мақсатты жасушаларға мРНҚ жеткізе алатын LNP-лерді әзірлеуде.
Осы жылы дебют жасаған Orbital Therapeutics сонымен қатар РНҚ терапиясын дамытудың негізгі бағыты ретінде қабылдайды.РНҚ технологиясы мен жеткізу механизмдерін біріктіре отырып, компания инновациялық РНҚ терапиясының тұрақтылығы мен жартылай ыдырау мерзімін ұзартуға және оларды әртүрлі жасушалар мен тіндерге жеткізуге болатын бірегей РНҚ технологиялық платформасын құруды күтеді.
Тарихи сәтте РНҚ терапиясының жаңа түрі пайда болады
Ағымдағы жылдың 21 желтоқсанындағы жағдай бойынша РНҚ терапиясы саласында 30 озық компания (бір компания екі рет қаржыландыру алды) тартылған, қаржыландырудың жалпы сомасы 1,74 млрд АҚШ долларын құрайтын 31 бастапқы кезеңдегі қаржыландыру іс-шарасы (толығырақ мақаланың соңындағы әдістемені қараңыз) өткізілді.Бұл компаниялардың талдауы көрсеткендей, инвесторлар РНҚ терапиясының әлеуетін толық іске асыру және пациенттерге көбірек пайда әкелу үшін РНҚ терапиясының көптеген мәселелерін шешеді деп күтілетін озық компанияларға оптимистік көзқараспен қарайды.
РНҚ терапиясының мүлдем жаңа түрлерін дамытатын келешек компаниялар бар.Дәстүрлі олигонуклеотидтерден, РНҚ немесе иРНҚ-дан айырмашылығы, осы компаниялар жасаған РНҚ молекулаларының жаңа түрлері бар терапиялардың тар мойнынан өтеді деп күтілуде.
Циркулярлы РНҚ - бұл саладағы ыстық нүктелердің бірі.Сызықтық мРНҚ-мен салыстырғанда Orna Therapeutics деп аталатын озық компания жасаған айналмалы РНҚ технологиясы туа біткен иммундық жүйе мен экзонуклеазалар тарапынан танудан аулақ бола алады, бұл иммуногенділікті айтарлықтай төмендетіп қана қоймайды, сонымен қатар жоғары тұрақтылыққа ие.Сонымен қатар, сызықтық РНҚ-мен салыстырғанда, дөңгелек РНҚ-ның бүктелген конформациясы кішірек, ал дөңгелек РНҚ-ны бірдей LNP-мен жүктеуге болады, бұл РНҚ терапиясының жеткізу тиімділігін арттырады.Бұл мүмкіндіктер РНҚ терапевтикасының потенциалы мен беріктігін жақсартуға көмектесуі мүмкін.
Биыл компания 221 миллион АҚШ доллары көлеміндегі B сериялы қаржыландыру кезеңін аяқтады, сонымен қатар зерттеу және3,5 миллиард АҚШ долларына дейін Merck-пен даму бойынша ынтымақтастық.Сонымен қатар, Orna жануарларда CAR-T терапиясын тікелей жасау үшін дөңгелек РНҚ пайдаланады, бұл дәлелдемені толтырады.тұжырымдамасы.
Дөңгелек РНҚ-дан басқа, өзін-өзі күшейтетін мРНҚ (samRNAs) технологиясы да инвесторлардың қолдауына ие болды.Бұл технология РНҚ вирустарының өзін-өзі күшейту механизміне негізделген, ол цитоплазмада samRNA тізбегінің репликациясын индукциялай алады, мРНҚ терапиясының экспрессиялық кинетикасын ұзартады, осылайша енгізу жиілігін азайтады.Дәстүрлі сызықтық мРНҚ-мен салыстырғанда, samRNA шамамен 10 есе төмен дозаларда ұқсас ақуыз экспрессия деңгейін сақтай алады.Осы жылы осы кен орнын дамытуға бағытталған RNAimmune A сериясы бойынша 27 миллион АҚШ долларын қаржыландыру алды.
tRNA технологиясы да асыға күтуге тұрарлық.tRNA негізіндегі терапия жасуша ақуызды жасаған кезде дұрыс емес тоқтату кодонын «елемей» алады, осылайша қалыпты толық ұзындықтағы ақуыз өндіріледі.Байланысты ауруларға қарағанда тоқтау кодондарының түрлері әлдеқайда аз болғандықтан, тРНҚ терапиясы көптеген ауруларды емдей алатын жалғыз терапияны әзірлеу мүмкіндігіне ие.Осы жылы tRNA терапиясына бағытталған hC Bioscience A сериясын қаржыландыруға барлығы 40 миллион АҚШ долларын жинады.
Eпилог
Жаңадан дамып келе жатқан емдеу үлгісі ретінде РНҚ терапиясы соңғы жылдары қарқынды дамуға қол жеткізді және көптеген терапиялар мақұлданды.Өнеркәсіптегі соңғы жаңалықтардан, ең озық РНҚ терапиялары мұндай терапиялар емдей алатын аурулардың ауқымын кеңейтіп, мақсатты жеткізудегі әртүрлі тығырықтарды жеңіп, тиімділік пен ұзақ мерзімділік бойынша қолданыстағы терапияның шектеулерін еңсеру үшін жаңа РНҚ молекулаларын дамытып жатқанын көруге болады.көптеген қиындықтар.РНҚ терапиясының осы жаңа дәуірінде бұл озық компаниялар алдағы бірнеше жылда саланың басты назарына айналуы мүмкін.
Қосымша тауарлар:
https://www.foreivd.com/cell-direct-rt-qpcr-kit-taqman-product/
https://www.foreivd.com/cell-direct-rt-qpcr-kit-direct-rt-qpcr-series/
Жіберу уақыты: 27 желтоқсан 2022 ж