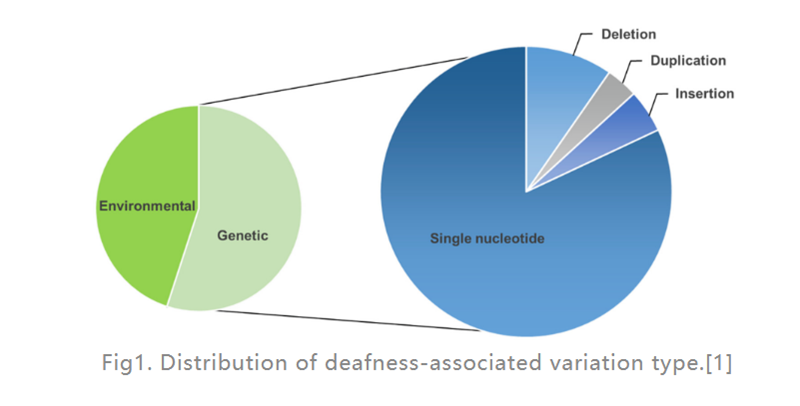
Есту қабілетінің жоғалуы (HL) - адамдарда ең көп таралған сенсорлық мүгедектік ауруы.Дамыған елдерде балалардың тілге дейінгі саңыраулық жағдайларының шамамен 80% генетикалық факторларға байланысты.Ең жиі кездесетіні бір генді ақаулар (1-суретте көрсетілгендей), 124 гендік мутация адамның синдромдық емес есту қабілетінің жоғалуымен байланысты екені анықталды, қалғандары қоршаған орта факторларынан туындайды.Кохлеарлық имплант (ішкі құлаққа орналастырылған, есту нервіне тікелей электрлік ынталандыруды қамтамасыз ететін электронды құрылғы) ауыр HL емдеудің ең тиімді нұсқасы болып табылады, ал есту аппараты (дыбыс толқындарын түрлендіретін және күшейтетін сыртқы электрондық құрылғы) орташа ауырлықтағы HL бар науқастарға көмектесе алады.Дегенмен, қазіргі уақытта тұқым қуалайтын HL (GHL) емдеуге арналған препараттар жоқ.Соңғы жылдары гендік терапия ішкі құлақ дисфункциясын емдеудің перспективалы тәсілі ретінде көбірек назар аударды.
1-сурет.Саңыраулықпен байланысты вариация түрінің таралуы.[1]
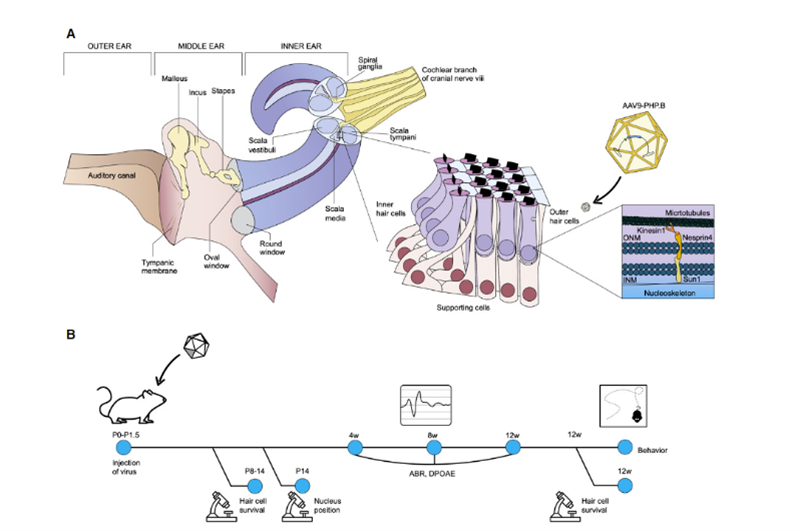
Жақында Солк институтының және Шеффилд университетінің ғалымдары тұқым қуалайтын кереңдіктің in vivo гендік терапиясын қолданудың кең перспективаларын көрсететін «Молекулалық терапия – әдістер және клиникалық даму» [2] зерттеу нәтижесін жариялады.Солк институтының ғылыми-зерттеу профессорының ассистенті және Уэйтт Жетілдірілген биофотоника орталығының директоры Ури Манор өзінің есту қабілетінің ауыр жоғалтуымен туылғанын және есту қабілетін қалпына келтіру керемет сыйлық болатынын айтты.Оның алдыңғы зерттеулері Eps8 актинді байланыстыру және жабу әрекеттері бар актинді реттеуші ақуыз екенін көрсетті;кохлеарлы шаш жасушаларында MYO15A, WHIRLIN, GPSM2 және GNAI3 бар Eps8 түзетін ақуыз кешені негізінен көп бөлігінде болады. MYO15A-мен бірге қысқа стереоцилия ұштарында BAIAP2L2 локализацияланған ұзын стереоцилиялардың ұштары шаш байламдарын ұстау үшін қажет.Сондықтан Eps8 қалыпты есту функциясы үшін өте қажет шаш жасушаларының стереоцилиясының ұзындығын реттей алады;Eps8 жойылуы немесе мутациясы қысқа стереоцилияға әкеледі, бұл дыбысты миды қабылдау үшін электрлік сигналдарға дұрыс түрлендіруге қабілетсіз етеді, бұл өз кезегінде кереңдікке әкеледі..Сонымен бірге, Шеффилд университетінің профессоры Уолтер Маркотти әріптесі, Eps8 болмаған кезде шаш жасушалары қалыпты түрде дами алмайтынын анықтады.Бұл зерттеуде Манор мен Маркотти стереоцилиарлы жасушаларға Eps8 қосу олардың қызметін қалпына келтіре алатынын және өз кезегінде тышқандардың есту қабілетін жақсарта алатынын зерттеу үшін бірігіп жұмыс жасады.Зерттеу тобы Eps8-/- жаңа туған P1-P2 тышқандарының кохлеясына жабайы типті EPS8 бар кодтау тізбегін жеткізу үшін адено-ассоциирленген вирус (AAV) Anc80L65 векторын дөңгелек терезе мембранасының инъекциясы арқылы пайдаланды;тінтуірдің кохлеарлы шаш жасушаларында стереоцилиялардың қызметі олар жетілгенге дейін қалпына келтірілді;және жөндеу әсері бейнелеу технологиясымен және стереоцилияны өлшеумен сипатталды.Нәтижелер Eps8 стереоцилия ұзындығын арттырғанын және төмен жиілікті жасушаларда шаш жасушаларының жұмысын қалпына келтіретінін көрсетті.Олар сондай-ақ, уақыт өте келе жасушалардың осы гендік терапия арқылы құтқарылу қабілетін жоғалтқанын анықтады.Бұдан шығатын қорытынды, бұл емдеуді жатырда енгізу қажет болуы мүмкін, өйткені тышқандар туылғаннан кейін Eps8-/- шаш жасушалары жетілген немесе қалпына келмейтін зақымданулар жинақталған болуы мүмкін.«Eps8 - әртүрлі функциялары бар ақуыз және әлі де зерттейтін көп нәрсе бар», - деді Манор.Болашақ зерттеулер әртүрлі даму кезеңдерінде есту қабілетін қалпына келтіруге Eps8 гендік терапиясының әсерін зерттеуді және емдеу мүмкіндіктерін ұзарту мүмкіндігін зерттеуді қамтиды.Кездейсоқ, 2020 жылдың қарашасында Израильдегі Тель-Авив университетінің профессоры КаренБ Аврахам EMBO Molecular Medicine журналында [3] зиянсыз синтетикалық адено-ассоциирленген AAV9-PHP вирусын жасау үшін инновациялық гендік терапия технологиясын қолдана отырып, өз нәтижелерін жариялады.B, Syne4-/- тышқандарының шаш жасушаларындағы ген ақауы тышқандардың ішкі құлағына Syne4 кодтау тізбегін тасымалдайтын вирусты енгізу арқылы жөнделді, бұл оның шаш жасушаларына енуіне және тасымалданатын генетикалық материалды босатып, олардың жетілуіне және қалыпты жұмыс істеуіне мүмкіндік береді (2-суреттегідей).
2-сурет.Корти органы мен несприн-4 жасушалық қызметіне назар аудара отырып, ішкі құлақ анатомиясының схемалық көрінісі.
Емдеу үшін кез келген мутацияға ұшыраған гендерді енгізу, жою немесе түзету (яғни аурудағы генетикалық өзгерістерді бақылау) арқылы тұқым қуалайтын ауруларды гендік деңгейде емдеу мақсатына жету үшін гендік терапияны қолданудың жоғары клиникалық әсері бар екенін көруге болады.қолдану перспективалары.Генетикалық жетіспейтін кереңдікке арналған қазіргі гендік терапия әдістерін келесі санаттарға бөлуге болады:
генді ауыстыру
Генді ауыстыру ақаулы генді геннің қалыпты немесе жабайы түрдегі көшірмесімен анықтауға және ауыстыруға негізделген гендік терапияның ең «қарапайым» түрі болып табылады.Везикулярлық глутамат тасымалдаушы 3 (VGLUT3) генінің жойылуынан туындаған есту қабілетінің жоғалуына арналған ішкі құлақтың гендік терапиясының алғашқы табысты зерттеуі;Ішкі құлақ шаш жасушаларында (IHCs) экзогендік VGLUT3 шамадан тыс экспрессиясының AAV1 арқылы жеткізілуі есту қабілетінің тұрақты қалпына келуіне, таспаның синаптикалық морфологиясының жартылай қалпына келуіне және конвульсиялық жауаптарға әкелуі мүмкін [4].Дегенмен, жоғарыдағы кіріспеде сипатталған AAV-жеткізілген екі генді ауыстыруды қамтитын мысалдарда есту қабілетінің жоғалуының тұқым қуалайтын бұзылыстарының гендік жойылуының белгілі бір түрлері үшін қолданылатын тінтуір үлгілері адамдардан уақытша ерекшеленетінін және P1 тышқандарында ішкі құлақтың дамудың жетілген сатысында екенін атап өту маңызды.Керісінше, адамдар жетілген ішкі құлақпен туылады.Бұл айырмашылық жетілген тінтуірдің құлақтарына гендік терапия жүргізілмейінше, тінтуір нәтижелерін адамның тұқым қуалайтын кереңдік ауруларын емдеуге қолдану мүмкіндігін болдырмайды.
Гендік өңдеу: CRISPR/Cas9
«Генді ауыстырумен» салыстырғанда, генді өңдеу технологиясының дамуы генетикалық ауруларды тамырдан емдеудің таңын ашты.Маңыздысы, генді редакциялау әдісі доминантты тұқым қуалайтын кереңдік ауруларына жарамсыз дәстүрлі шамадан тыс экспрессиялық генотерапия әдістерінің кемшіліктерін және шамадан тыс экспрессия әдісі ұзаққа созылмайтын проблеманы толтырады.Қытайлық зерттеушілер AAV-SaCas9-KKH-Myo6-g2 гендік өңдеу жүйесін пайдаланып Myo6WT/C442Y тышқандарындағы Myo6C442Y мутант аллелін арнайы нокаутқа түсіргеннен кейін және нокауттан кейін 5 ай ішінде тышқандар Модельдің есту функциясы қалпына келтірілді;сонымен қатар ішкі құлақтағы түк жасушаларының өмір сүру деңгейінің жақсарғаны, кірпікшелердің пішіні қалыпты болып, электрофизиологиялық көрсеткіштердің түзетілгені де байқалды [5].Бұл Myo6 генінің мутациясынан туындаған тұқым қуалайтын кереңдікті емдеу үшін CRISPR/Cas9 технологиясын қолданатын әлемдегі алғашқы зерттеу және бұл тұқым қуалайтын кереңдікті емдеуге арналған генді өңдеу технологиясының маңызды зерттеу прогресі.Емдеудің клиникалық аудармасы берік ғылыми негіз береді.
Гендік терапияны жеткізу әдістері
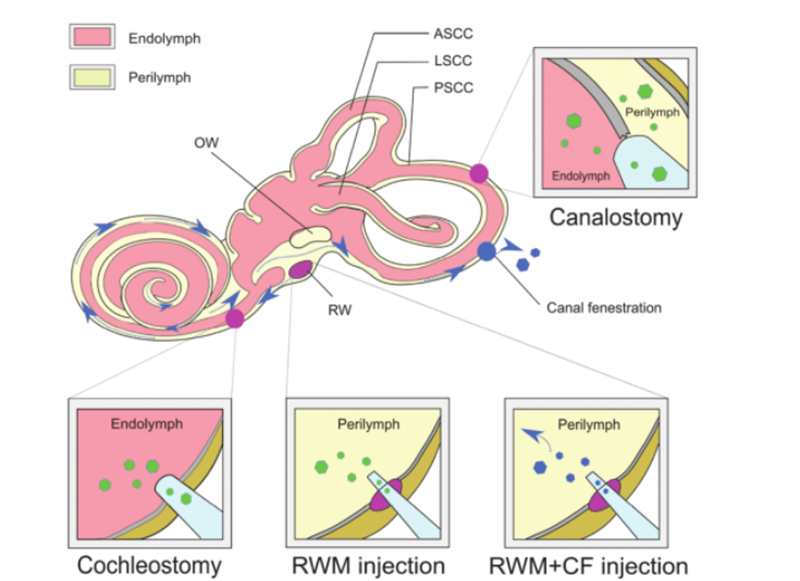
Гендік терапия сәтті болуы үшін жалаңаш ДНҚ молекулалары олардың гидрофильділігіне және фосфат топтарының теріс зарядына байланысты жасушаларға тиімді ене алмайды және толықтырылған нуклеин қышқылы молекулаларының тұтастығын қамтамасыз ету үшін қауіпсіз және тиімді әдіс таңдалуы керек.Қосымша ДНҚ мақсатты жасушаға немесе тінге жеткізіледі.AAV жоғары инфекциялық әсері, төмен иммуногенділігі және тіндердің әртүрлі түрлеріне кең тропизмі арқасында ауруды емдеуде жеткізу құралы ретінде кеңінен қолданылады.Қазіргі уақытта ғылыми-зерттеу жұмыстарының үлкен бөлігі тінтуірдің кохлеясының әртүрлі жасуша түрлеріне қатысты AAV әртүрлі субтиптерінің тропизмін анықтады.Жасушаға тән промоторлармен біріктірілген AAV жеткізу сипаттамаларын пайдалану мақсаттан тыс әсерлерді азайтуы мүмкін жасушаға тән экспрессияға қол жеткізуге болады.Сонымен қатар, дәстүрлі AAV векторларына балама ретінде жаңа синтетикалық AAV векторлары үнемі әзірленуде және ішкі құлақта жоғары трансдукциялық қабілетін көрсетеді, олардың ішінде AAV2/Anc80L65 ең көп қолданылады.Вирустық емес жеткізу әдістерін одан әрі физикалық әдістерге (микроинъекция және электропорация) және химиялық әдістерге (липидті, полимер негізіндегі және алтын нанобөлшектері) бөлуге болады.Екі тәсіл де тұқым қуалайтын кереңдік бұзылыстарын емдеуде қолданылған және әртүрлі артықшылықтар мен шектеулерді көрсетті.Көлік құралы ретінде гендік терапияны жеткізу құралына қоса, in vivo генді енгізуге арналған әртүрлі тәсілдер әртүрлі мақсатты жасуша түрлеріне, енгізу жолдарына және терапевтік тиімділікке негізделуі мүмкін.Ішкі құлақтың күрделі құрылымы мақсатты жасушаларға жетуді қиындатады және геномды өңдеу агенттерінің таралуы баяу.Қабықшалы лабиринт самай сүйегінің сүйек лабиринтінде орналасқан және оған кохлеарлық түтік, жартылай шеңберлі түтік, утрикул және баллон кіреді.Оның салыстырмалы оқшаулануы, ең аз лимфа айналымы және қаннан қан лабиринтінің тосқауылымен бөлінуі терапевтикалық препараттарды тек жаңа туған тышқандарға тиімді жүйелі жеткізуді шектейді.Гендік терапияға жарамды вирустық титрлерді алу үшін вирустық векторларды ішкі құлаққа тікелей жергілікті енгізу қажет.Белгіленген инъекция жолдарына [6] жатады: (1) дөңгелек терезе мембранасы (RWM), (2) трахеостомия, (3) эндолимфатикалық немесе перилимфатикалық кохлеостомия, (4) дөңгелек терезе мембранасы және түтік фенестрациясы (CF) (3-суреттегідей).
3-сурет.Ішкі құлаққа гендік терапияны жеткізу.
Клиникалық трансляциялық мақсаттарға негізделген гендік терапияда көптеген жетістіктерге қол жеткізілгенімен, гендік терапия генетикалық аурулары бар науқастарды емдеудің бірінші қатардағы нұсқасына айналмас бұрын, әсіресе қауіпсіз және тиімді векторларды және жеткізу әдісін әзірлеуде көп жұмыс істеу керек.Бірақ біз жақын болашақта емдеудің бұл түрлері жеке терапияның негізгі бөлігіне айналады және генетикалық бұзылулары бар адамдар мен олардың отбасыларының өміріне үлкен оң әсер етеді деп сенеміз.
Foregene сонымен қатар жылдам және РНҚ экстракциясынсыз кері транскрипция мен qPCR реакцияларын орындай алатын мақсатты гендер үшін жоғары өнімді скрининг жинағын іске қосты.
Өнім сілтемелері
Cell Direct RT-qPCR жинағы — Taqman/SYBR GREEN I
Өнім туралы қосымша ақпарат алу үшін хабарласыңыз:
Жіберу уақыты: 02 қыркүйек 2022 ж